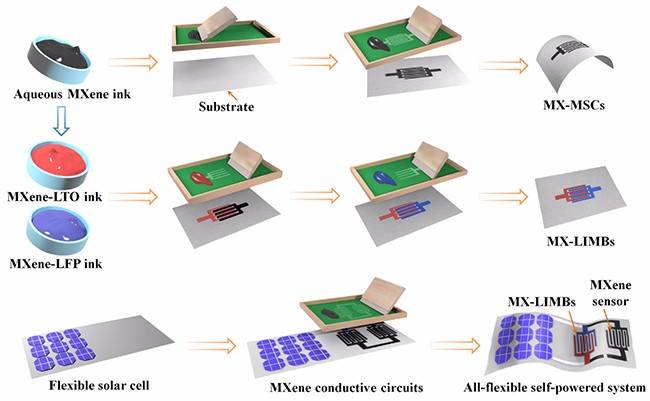
一、無負極二次鋰金屬電池設(shè)計的方式及關(guān)鍵點
隨著儲能行業(yè)的不斷發(fā)展,追求更高能量密度、更低成本、更安全、更穩(wěn)定的鋰電池已勢不可擋。盡管目前以石墨為負極的鋰離子電池(LIBs)在電子設(shè)備、電動汽車和智能電網(wǎng)存儲領(lǐng)域頗受重視,但其較低的能量密度明顯跟不上日益增長的使用需求。因此,鋰金屬負極又重回舞臺,以取代石墨負極,為電池提供更高的能量密度。鋰金屬負極的理論比容量為3820 mA h/g,是石墨負極的10倍(372 mA h/g)。然而,鋰金屬負極在工作的時候,常常伴隨著鋰的均勻沉積、以及形成不穩(wěn)定的固體電解質(zhì)界面層(SEI),導(dǎo)致鋰在電鍍/剝離后生長大量的枝晶,引發(fā)電池的安全問題,縮短電池壽命。因此,如何避免以上問題,在增加能量密度的同時提高電池安全性能,是研究者們正在思考的新命題。
其中一個很新穎的想法是使用Anode-Free系統(tǒng)。原則上,如果從正極中脫出的鋰離子,可以可逆地在銅集流體上進行電鍍和剝離,則可以組裝出Cu/隔膜/正極/Al型的可充電鋰金屬電池。由于這種電池中沒有活性負極,因此被稱為“無負極可充電鋰金屬電池”(AFLMB)。這里的“無負極”并不是說電池中真的沒有負極,而指的是無負極活性物質(zhì)作為Li+的宿主。因此,這種設(shè)計可以減少電池的重量和空間,與傳統(tǒng)鋰離子電池相比,AFLMB的能量密度將顯著提升。如果該類型的電池能進入工業(yè),那將節(jié)省與負極生產(chǎn)(包括漿料制備、漿料涂層和干燥)工序相關(guān)的成本和時間。然而,除了上述優(yōu)點外,AFLMB有一個致命的缺點,那就是其SEI非常不穩(wěn)定,因此會消耗大量的活性鋰和電解質(zhì),因此庫侖效率(CE)和循環(huán)容量保留率較低。
在這類無負極電池系統(tǒng)中實現(xiàn)穩(wěn)定的鋰電鍍/剝離過程,其關(guān)鍵在于設(shè)計出性能更好的電解質(zhì)。而設(shè)計電解質(zhì)時,首先應(yīng)考慮鋰鹽的選擇、溶劑和濃度的控制。固體電解質(zhì)、無機電解質(zhì)以及混合離子液體電解質(zhì)雖然可以抑制鋰枝晶生長,但其在室溫下具有低導(dǎo)電性和高界面電阻,動力學(xué)性能受到很大限制。傳統(tǒng)鋰離子電池中采用的電解質(zhì)為1 M LiPF6,電解液為碳酸鹽基溶劑,然而碳酸鹽電解質(zhì)體系與鋰金屬的相容性較差,極易導(dǎo)致鋰枝晶生長,因此也不能用在AFLMB中。近來,Zhang等人采用一種高濃度的醚基電解質(zhì)(4 M LiFSI/DME)來穩(wěn)定鋰負極(Nat. Commun. 2015, 6, 6362)。的確,高濃度電解質(zhì)可以提高正負極氧化物的穩(wěn)定性、無游離溶劑、高陰離子含量、提高活性鋰離子數(shù)量。然而,醚基溶劑的抗氧化能力較差且成本高,無法滿足高壓正極的穩(wěn)定運行,因此實用性不高。如果從成本角度考慮,六氟磷酸鋰(LiPF6)無疑是最好的選擇。
二、如何設(shè)計電解液組成來穩(wěn)定電化學(xué)循環(huán)
國立臺灣科技大學(xué)Bing-Joe Hwang等人采用高濃度LiPF6 in EC/DEC(1:1 v/v)電解液,搭配50%的氟乙烯碳酸鹽(FEC)稀釋劑,將NMC//Cu這種無負極鋰金屬電池的循環(huán)壽命提高到1066小時以上。
2.1 探究電解液濃度對電池穩(wěn)定性的影響
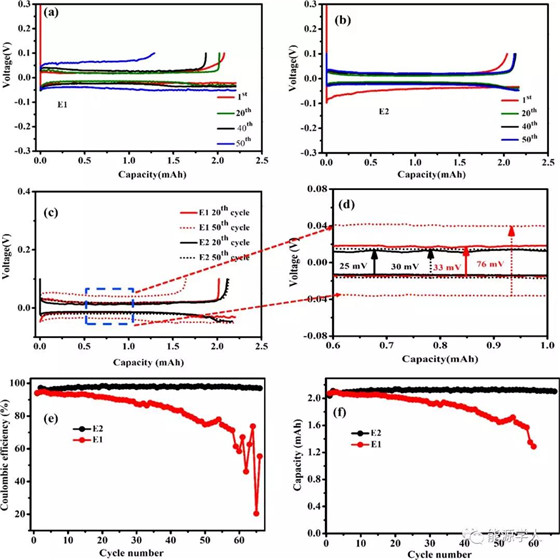
為了理解電池的極化、循環(huán)、庫倫效率,作者首先進行了Li||Cu半電池測試。上圖中E1.5表示1.5 M LiPF6,E2表示2 M LiPF6,E3表示3 M LiPF6,E4表示4 M LiPF6。從循環(huán)的CE中,可以理解鋰電鍍/剝離過程中的活性鋰的消耗速率、及電解質(zhì)的分解程度。E1和E2情況下的電池在0.2mA/cm2電流密度下的CE趨勢如上圖e所示,由于半電池中的負極為鋰箔,則CE的本質(zhì)為由于電解質(zhì)分解而導(dǎo)致銅集流體上的鋰損耗。在圖e中,E1和E2在一開始時的庫倫效率均為~94%,這表明,無論電解質(zhì)類型和濃度如何,電池的第一個循環(huán)中幾乎沒有什么差異。然而,在含有E1電解質(zhì)的電池中,CE衰減很快,僅僅幾個循環(huán),就開始出現(xiàn)波動。同樣的趨勢從圖c和圖d中也可看出,僅僅50個循環(huán),E1電池的極化電壓就升高至76 mV,這表明,在經(jīng)過幾個電鍍/剝離循環(huán)后,E1電池中的死鋰沉積較厚,從而在銅表面快速生長鋰枝晶,導(dǎo)致高電阻層的形成,增大離子和電子擴散電阻,從而使極化電壓迅速上升。上述這種現(xiàn)象也再一次證明了商業(yè)1 M LiPF6 EC/DEC 1:1 v/v電解質(zhì)于AFLMB不兼容。與之對比,E2電池可以穩(wěn)定循環(huán)超過1066h,CE一直維持在98%,極化電壓僅為30 mV,首次循環(huán)的極化率很高,第二次循環(huán)后極化率下降,這說明由高濃度電解質(zhì)E2可以形成更加穩(wěn)定的SEI。作者將性能優(yōu)異的原因歸功于FEC稀釋劑和高濃度電解質(zhì)中的鹽協(xié)同作用,形成堅固的SEI,防止鋰枝晶的形成。
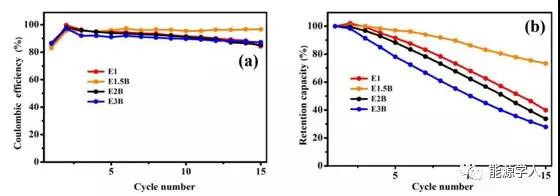
上圖為無負極Cu ‖ NMC紐扣電池在0.2 mA/cm2下運行時,不同濃度電解質(zhì)的庫倫效率和容量保留率對比(B表示不含F(xiàn)EC稀釋劑)。
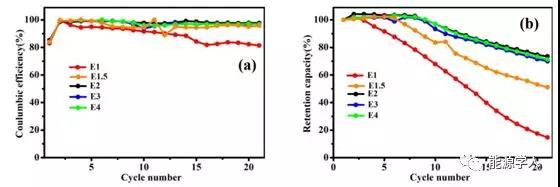
上圖為無負極Cu ‖ NMC紐扣電池在0.2 mA/cm2下運行時,不同濃度電解質(zhì)的庫倫效率和容量保留率對比(含有FEC稀釋劑)。
三、銅負極表面SEI的分析,探究電池能循環(huán)穩(wěn)定的原因
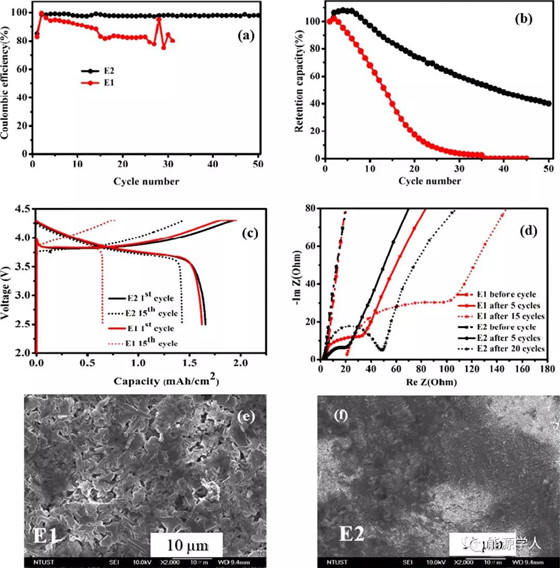
無負極Cu||NMC紐扣電池正極為NMC111,負極為Cu箔,電解液為不同濃度的LiPF6 in EC/DEC (1:1 v/v ratio),以FEC為稀釋劑。即便有文獻顯示碳酸鹽溶劑(EC/EMC (3:7 wt %))在第一次充電后會損失77%(J. Electrochem. Soc. 2014, 161, A827?A830.),作者的實驗還是表示,不管電解質(zhì)類型如何,在AFLMB首次循環(huán)中,電解液損失幾乎只有14%。但是15圈以后,E1電解質(zhì)的損耗高達60%(上圖c)。如上圖a所示,使用E1電解質(zhì)的AFLMB電池,其CE迅速下降(<90%),幾個循環(huán)后開始波動,這可能由于在連續(xù)電鍍/剝離過程中,游離溶劑與活性鋰離子反應(yīng)導(dǎo)致活性鋰耗盡。另外,傳統(tǒng)碳酸鹽電解質(zhì)中形成的SEI層由電解質(zhì)溶劑分解而成,因此消耗電解質(zhì)也是另一個原因。
相反,如上圖b,c所示,高濃度電解質(zhì)E2即使在第15個循環(huán)時,CE仍保持在86%以上。如圖2b所示,即使經(jīng)過50個循環(huán),ACE仍超過97.8%,這是目前已知的碳酸鹽基溶劑在AFLMB中的最高值。為了進一步了解高濃度LiPF6和FEC稀釋劑的協(xié)同作用對穩(wěn)定無負極電池的正面影響,作者采用電化學(xué)阻抗譜(EIS)研究了電解質(zhì)/電極界面行為。從上圖d也可以看出,含有E1的電池,在15個循環(huán)期間,電阻非常高,這表明與死鋰反應(yīng)的SEI很厚,增加電子和離子擴散電阻。從上圖e中的掃描電鏡形貌也很容易的觀察到死鋰粉體。然而,即使經(jīng)過20個循環(huán),帶有E2電解質(zhì)的電池明顯電阻較低,這顯然證明了稀釋劑具有通過降低粘度來提高離子導(dǎo)電性的作用。
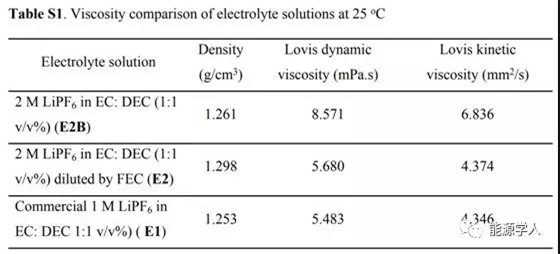
在上表中可以觀察到電解液的粘度對比,高濃度E2B電解質(zhì)的Lovis動態(tài)粘度為8.571mPa·s,高于加入稀釋劑厚的E2電解質(zhì)(5.680mPa·s)。
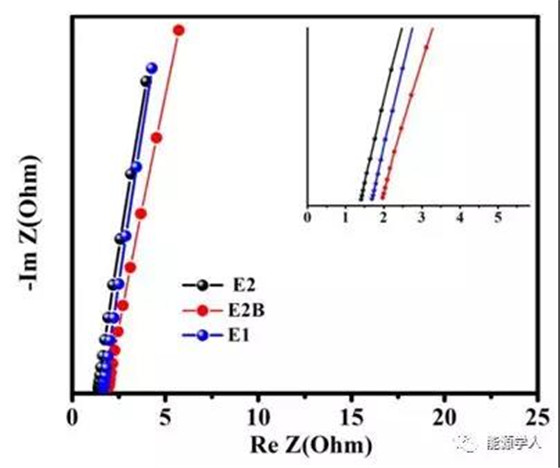
通過對比不銹鋼//不銹鋼電池的阻抗,可以看出不同電解液的離子導(dǎo)電性,如上圖所示。

電解質(zhì)的離子電導(dǎo)率是根據(jù)電阻(R)數(shù)據(jù)計算得出的,如上式所示,R表示電解質(zhì)溶液的電阻,ρ表示電阻率,L表示兩個電極之間的距離,A表示橫截面積。因此,溶液的離子電導(dǎo)率k與電阻率(ρ)的倒數(shù)有關(guān)。計算得到高濃度電解質(zhì)E2的離子導(dǎo)電率為1.34×10-3 s cm-1,高于E1 (1.12×10-3 s cm-1),高于E2B (9.54 × 10–4 S cm–1)。

一般來說,稀釋劑的作用主要是降低粘度和增加電導(dǎo)率,但由于離子對的電荷中性,其對高濃度電解液的離子遷移率并沒有很大影響。它不會改變高濃度電解質(zhì)的特性,因此SEI的形成主要是由溶劑化鹽絡(luò)合物的分解產(chǎn)物組成。上圖a中位于714 cm-1處的拉曼特征峰,屬于EC中的C═O彎曲振動;隨著LiPF6濃度的增加,其強度逐漸降低,并向741 cm-1處移動,這是PF6–的特征峰。同樣,在圖a中還出現(xiàn)了位于893 cm–1處的EC分子特征峰,隨著LiPF6濃度的增加,該峰逐漸被905 cm–1處取代,但這仍舊屬于EC分子的特征峰。這表示FEC是良好的稀釋劑,即使由于溶液中存在FEC而出現(xiàn)新的峰,但溶液結(jié)構(gòu)仍不受稀釋劑的影響。因此,由于稀釋劑不影響溶液溶劑化結(jié)構(gòu)的特性,SEI的形成機理仍舊主要是由陰離子的分解產(chǎn)物所決定的,與市售電解質(zhì)E1相比,高濃度電解質(zhì)中游離溶劑的量明顯減少。此外,從圖b (I–III)的擬合曲線來看,隨著鹽濃度的增加,位于893cm-1處的自由溶劑EC峰強度逐漸減小,并向更高的波段移動。
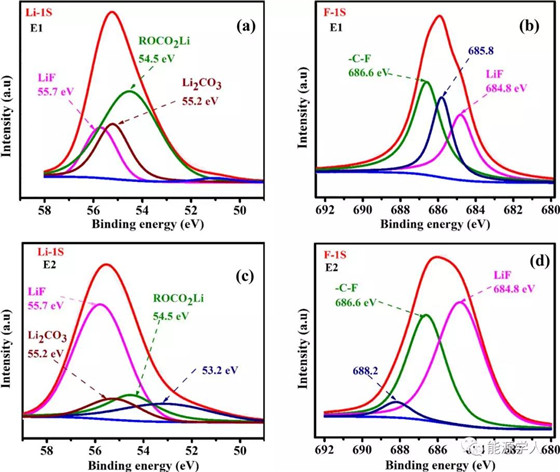
為了更好的了解銅負極表面SEI的化學(xué)成分,作者對5個循環(huán)后完全放電的負極進行XPS表征。上圖a-d分別顯示了使用E1電解質(zhì)的Li-1s、使用E1電解質(zhì)的F-1s、使用E2電解質(zhì)的Li-1s和使用E2電解質(zhì)的F-1s XPS特征峰。圖a、c所示的Li-1s光譜中,55.2、55.4和55.7eV處的峰分別屬于Li2CO3、ROCO2Li和LiF。同樣的,圖b、d所示的F-1s光譜中,684.8和686.6 eV處的峰分別屬于LiF和C–F。但是,也有一些峰尚未對應(yīng)特定的化合物或官能團,例如L-1s中的53.2 eV(圖c)、使用E2電解質(zhì)的F-1s中的688.2 eV(圖d)和使用E1電解質(zhì)的F-1s中的685.8 eV(圖4b)。在圖a的光譜中,使用E1電解質(zhì),可以明顯地觀察到,有機物的峰值強度很高,例如在Li-1s光譜中的ROCO2Li和在O-1s和C-1s光譜中的?CH2–CH2O, C═O,表明SEI的主要成分來自溶劑分解。而在高濃度E2電解質(zhì)中,SEI膜中含有無機物(如LiF)的高峰值強度。圖c,d中LiF光譜強度的增加可能是由鹽分解引起的陰離子一次還原,這是陰離子衍生SEI形成的證據(jù)。一般來說,在高濃度E2電解質(zhì)的SEI膜組成中,其他無機物如Li2O和Li2CO3也支持這一證據(jù)。

此外,作者還研究了高濃度電解質(zhì)對不同上限電壓的穩(wěn)定性。可以看出,當(dāng)上限截止電壓從4.3 V變?yōu)?.1 V和從4.3 V變?yōu)?.5 V時,E1電解質(zhì)的放電容量有顯著差異,如上圖c,d所示。截止電壓上限越低,保留容量越高,這與理論預(yù)期相符。然而,在高濃度電解質(zhì)中,無論上述電壓變化之間的變化如何,保留容量幾乎保持不變,如圖a,b所示,這表示高濃度電解質(zhì)在高電壓下的穩(wěn)定性更好。
先拋出這項工作的關(guān)鍵性結(jié)論:
1. 無負極鋰金屬電池(AFLMB)作為一種新穎的儲能系統(tǒng),盡管能量密度相對提高,但一直找不到適合的電解液。常見的高濃度醚類電解質(zhì)不僅成本高,而且不能耐高壓,因此急需找到一種低成本、高穩(wěn)定性的電解質(zhì)。在本文中,作者采用高濃度LiPF6 in EC/DEC(1:1 v/v)電解液,搭配50%的氟乙烯碳酸鹽(FEC)稀釋劑,將NMC||Cu這種無負極鋰金屬電池的循環(huán)壽命提高到1066小時以上。
2. 在Li||Cu半電池測試中,不論電解質(zhì)的類型和濃度如何,電池的首次庫倫效率均為~94%,但是,僅僅幾個循環(huán)后,低濃度的電解質(zhì)便開始快速衰減,無法穩(wěn)定運行。此外,作者發(fā)現(xiàn)50個循環(huán)后,低濃度電解質(zhì)的電池極化電壓就升高至76 mV,這表明,在經(jīng)過幾個電鍍/剝離循環(huán)后,低濃度電解質(zhì)的電池中死鋰沉積較厚,從而在銅表面快速生長鋰枝晶,導(dǎo)致高電阻層的形成,增大離子和電子擴散電阻,從而使極化電壓迅速上升。
3. 在無負極Cu||NMC紐扣電池測試中,使用E1電解質(zhì)的AFLMB電池,其CE迅速下降(<90%),幾個循環(huán)后開始波動,這可能由于在連續(xù)電鍍/剝離過程中,游離溶劑與活性鋰離子反應(yīng)導(dǎo)致活性鋰耗盡。另外,傳統(tǒng)碳酸鹽電解質(zhì)中形成的SEI層由電解質(zhì)溶劑分解而成,因此消耗電解質(zhì)也是另一個原因,但高濃度的電解質(zhì)就沒有這個問題。